

背景介绍
2026年2月25日,伊利诺伊大学芝加哥分校、中国科学院分子细胞科学卓越创新中心等机构的研究人员合作,在《Nature》发表了题为“Human hippocampal neurogenesis in adulthood, ageing and Alzheimer’s disease”的研究论文。该研究利用先进的单细胞多组学测序技术,分析了从年轻成人到AD患者,再到拥有卓越记忆力的“超级老人”的35万个细胞核。研究不仅终结了“人类是否存在成人神经发生”的争议,更绘制了一幅宏大的分子图谱,揭示了认知韧性背后的表观遗传密码。
研究背景
困扰领域的两大核心谜题
海马体作为记忆与学习的核心中枢,其神经发生(神经干细胞生成新神经元)的命运一直是领域焦点,但两大谜题长期悬而未决:
1、成年人类海马神经发生是否存在?
2、神经发生如何影响衰老与AD?
为破解这些谜题,研究团队选取5个关键队列:认知完好的年轻人(YA)、认知正常的老年人(HA)、临床前期AD患者(PCI)、AD患者,以及“超级老人”(SA),通过单核RNA测序(snRNA-seq)和单核转座酶可及染色质测序(snATAC-seq),从转录组和表观组层面解析神经发生的分子机制。
核心突破
颠覆性发现改写神经科学认知
1、成年人类海马存在完整神经发生轨迹
研究通过多组学首次证实,成年人类海马齿状回存在从神经干细胞(NSCs)→神经母细胞→未成熟神经元→成熟颗粒神经元的完整发育轨迹。
单细胞转录组分析显示,神经干细胞表达高水平干细胞标志物,神经母细胞富集轴突、树突发育相关通路,未成熟神经元则聚焦突触功能与可塑性;而snATAC-seq进一步验证,神经干细胞中多能性相关区域染色质高度开放,神经元成熟标志物的染色质开放水平随分化逐步升高,完美复刻了神经发生的表观遗传调控规律。这一发现直接终结了长期争议,为人类神经再生研究奠定基础。
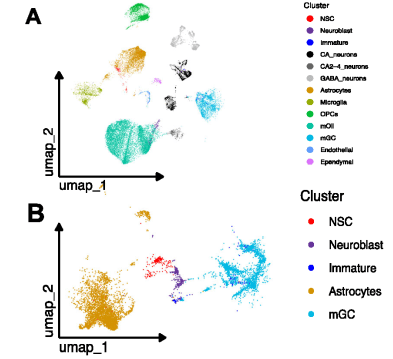
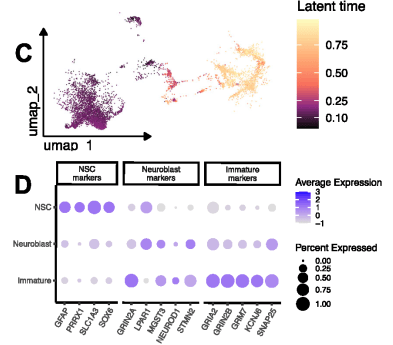 Fig 1 人类成年海马体神经发生轨迹编辑
Fig 1 人类成年海马体神经发生轨迹编辑
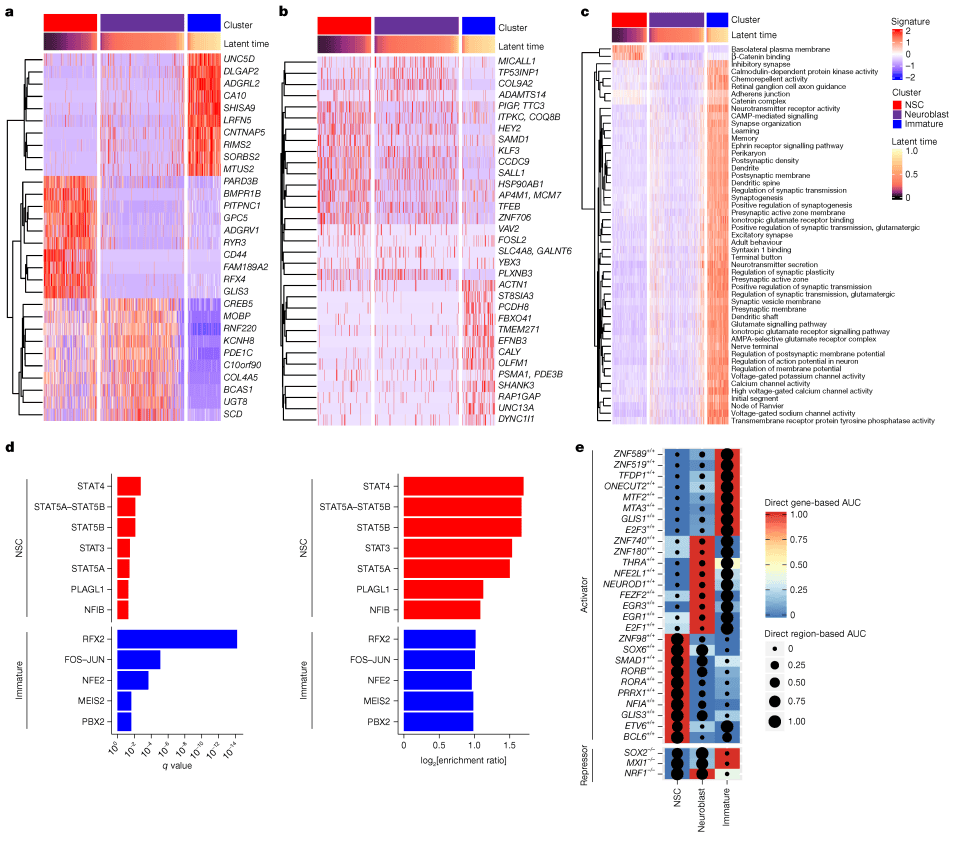 Fig 2 成人人类大脑神经发生的分子网络编辑
Fig 2 成人人类大脑神经发生的分子网络编辑
2、AD的早期预警信号:染色质可及性先于基因表达改变
研究发现,神经发生失调的核心驱动因素是染色质可及性变化,且这一改变早于基因表达差异,成为AD早期诊断与干预的全新靶点:
AD患者中神经干细胞数量异常增加,但神经母细胞和未成熟神经元数量显著减少,形成“干细胞堆积、成熟受阻”的异常状态
在PCI期,基因表达(DEGs)的变化微乎其微,但神经发生相关细胞的染色质开放性(DARs)已经发生了显著改变(关闭)
锌指转录因子家族和RFX家族基序的染色质可及性变化,是调控这一过程的关键,为AD的早期诊断和干预提供了全新靶点
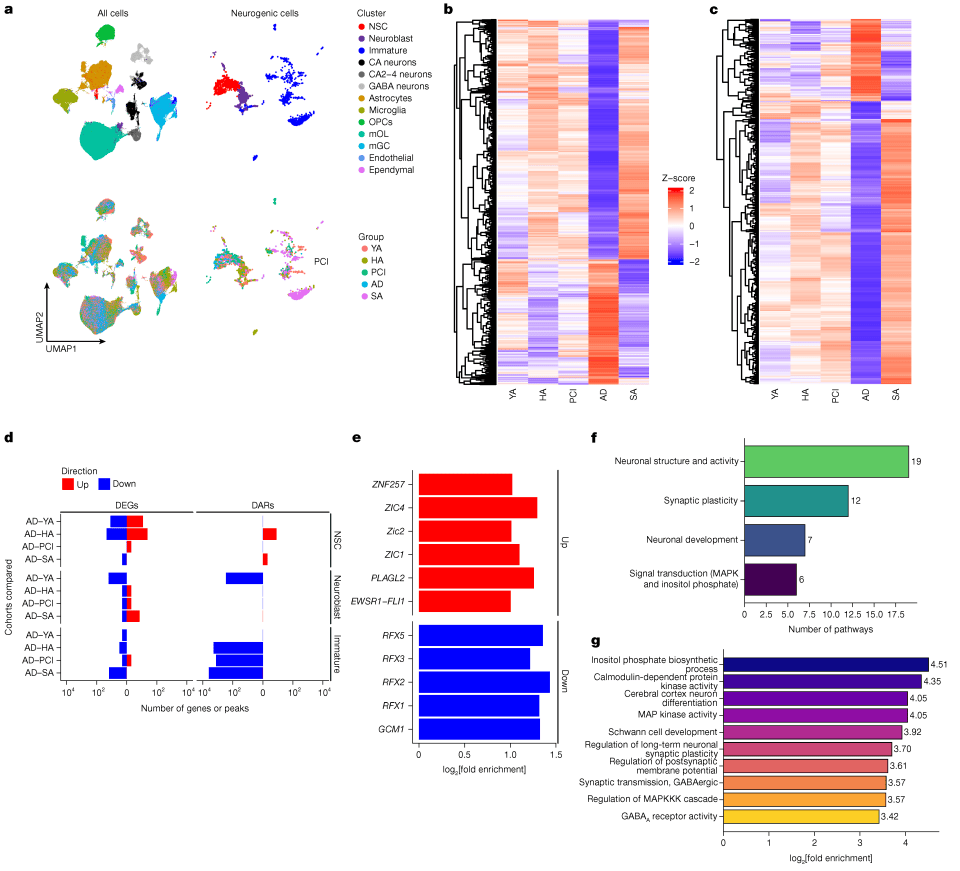 Fig 3 年龄和认知诊断的差异性表达与开放染色质编辑
Fig 3 年龄和认知诊断的差异性表达与开放染色质编辑
3、调控网络错乱:AD神经发生“受阻”的关键机制
利用SCENIC+算法,研究团队构建了不同状态下的增强子驱动的调控网络(eRegulons)。在AD中,驱动神经发生的正常转录因子网络(如ZNF98,RORB)活性减弱,而异常的激活因子(如RXRG,RARG)出现。PCI阶段展现出一种过渡状态,NSC中的阻遏蛋白(如SOX6,PAX6)表达上调,阻碍了分化进程。调控网络的错乱,解释了为何AD大脑中的神经干细胞虽然数量众多,却陷入了发育的死胡同。
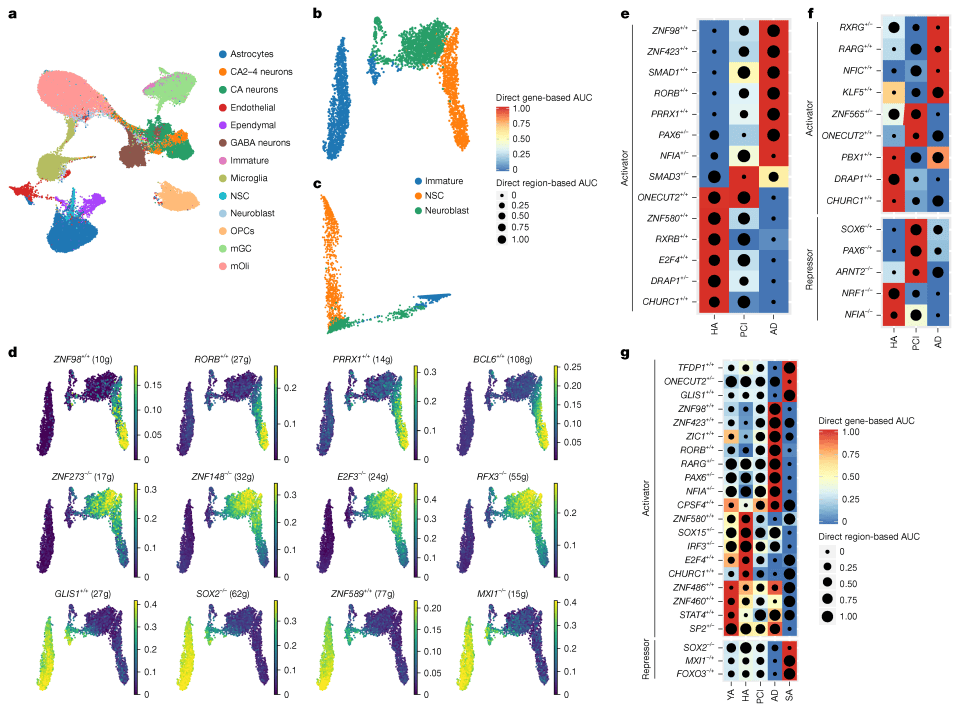 Fig 4 衰老和认知衰退中的基因调控网络编辑
Fig 4 衰老和认知衰退中的基因调控网络编辑
4、超级老人的“抗衰密码”:独特的神经发生韧性特征
“超级老人”之所以能抵御衰老和AD带来的认知衰退,核心在于其神经发生存在独特的“韧性特征”:
超级老人海马体中未成熟神经元数量是AD患者的2倍以上,神经母细胞数量也显著更多
SA的神经前体细胞维持了高水平的线粒体功能、突触传递相关基因表达,其染色质状态有效抵抗了衰老带来的“关闭”效应
超级老人拥有专属的增强子驱动调控网络(eRegulons),如未成熟神经元中的PROX1激活因子,神经干细胞中的ZNF423、ZIC1等,这些因子可能是维持认知韧性的关键分子。
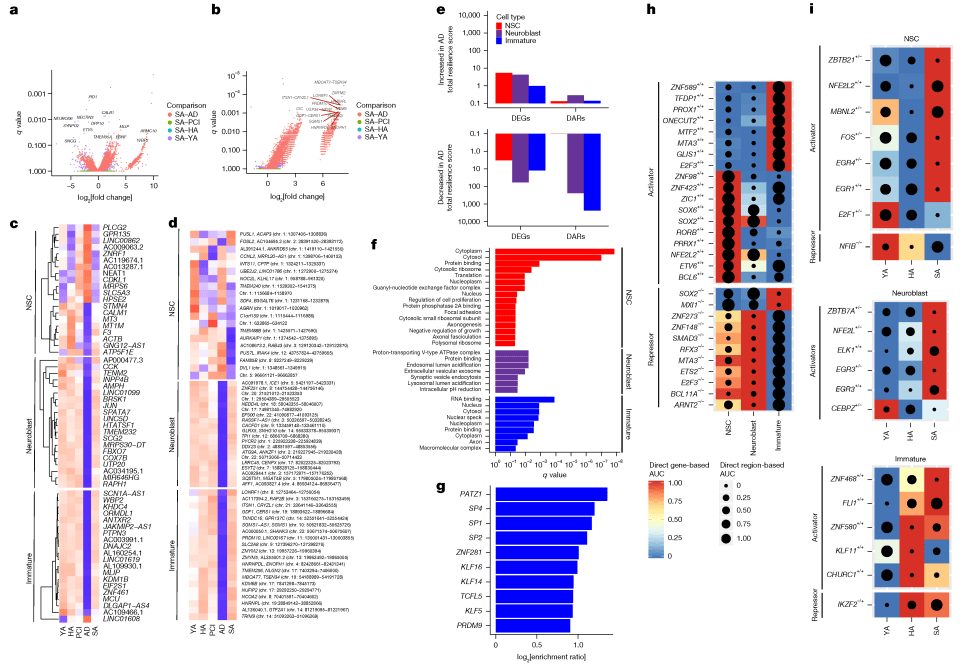 Fig 5 神经发生的韧性特征编辑
Fig 5 神经发生的韧性特征编辑
5、关键机制:细胞间通讯决定“成功衰老”与否
神经发生不是孤立的。研究分析了微环境中的星形胶质细胞和CA1神经元。研究还揭示,海马体认知功能的维持不仅依赖神经发生,还与细胞间的协同作用密切相关:正常衰老的核心特征是CA1神经元中神经传递、突触可塑性相关基因高表达,星形胶质细胞中FOS-JUN家族基序染色质可及性维持稳定;而认知衰退(PCI、AD)的关键在于,CA1神经元与星形胶质细胞、神经发生细胞之间的谷氨酸能通路、突触粘附通路(如NRXN1-NLGN)通讯减弱,导致神经网络功能紊乱。这一发现表明,认知衰老并非单一细胞类型的功能衰退,而是整个海马体微环境的协同失调,为多靶点干预提供了新思路。
 Fig 6 正常与病理衰老状态下的海马网络编辑
Fig 6 正常与病理衰老状态下的海马网络编辑
研究意义
为神经科学研究开辟全新方向
这项研究通过多组学技术与梯度队列设计,不仅终结了成年人类海马神经发生的长期争议,更构建了神经发生在衰老、AD进程中的分子调控图谱,其意义深远:
01、基础研究层面
明确了人类海马神经发生的完整轨迹与调控网络,为神经再生机制研究提供了全新的理论框架
02、临床转化层面
发现了AD早期诊断的潜在分子标志物与精准干预靶点,打破了传统AD治疗聚焦β-淀粉样蛋白清除的单一思路
03、抗衰老层面
解锁了超级老人的认知韧性密码,为开发延缓认知衰退、维持大脑健康的干预策略提供了直接参考
拜谱小结
拜谱生物作为国内领先的多组学技术服务公司,构建了完善成熟的技术服务体系。深度布局单细胞研究领域,可提供单细胞转录组测序、多组学数据整合分析等核心技术服务,同时涵盖蛋白质组学、修饰组学等关键技术平台。我们能通过转录组与蛋白组数据联动挖掘及深度机制解析,精准匹配海马神经发生、AD 机制探索、衰老认知研究等领域的需求,助力科研人员解析神经细胞亚群异质性、关键分子调控网络及细胞间互作机制等核心科学问题,从样本制备、实验检测到数据分析全链条赋能,冲刺高分文章!欢迎咨询合作,共同推进神经科学领域科研突破!
参考文献
Disouky A, et al. Human hippocampal neurogenesis in adulthood, ageing and Alzheimer's disease. Nature. 2026 Feb 25. doi: 10.1038/s41586-026-10169-4.