

背景介绍
在病毒致癌、肿瘤异质性等复杂疾病研究中,科研者常面临两大痛点:一是海量组学数据与临床表型难以建立可靠关联,二是高分研究的技术流程复杂、难以复现。
近期发表于《International Journal of Surgery》的Epstein-Barr病毒(EBV)致肾透明细胞癌(ccRCC)研究,成功构建了一套“因果推断→靶点筛选→转化验证”完整技术路线,为复杂疾病的机制研究与药物发现提供了可复用的方法论框架。

研究痛点
EBV与ccRCC的关联研究,两大难点:
EBV感染极为普遍,且ccRCC患者免疫状态复杂,难以区分“感染是病因还是结果”
病毒感染引发的分子级联反应涉及免疫、遗传、表观等多个层面,传统单一分析方法无法锁定核心驱动因子。
为突破这一瓶颈,研究团队构建了一套“因果推断→靶点筛选→转化验证”的技术路线,层层拆解EBV致ccRCC的分子路径。
从“关联”到“机制”
1、孟德尔随机化(MR)排除混杂因素
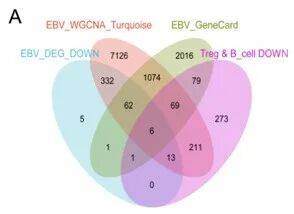
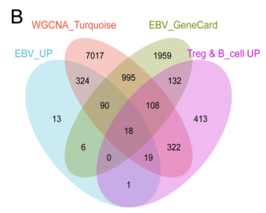
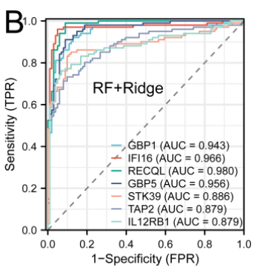
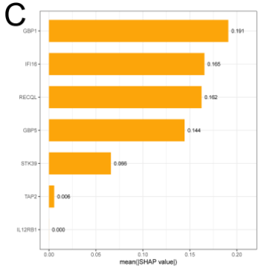
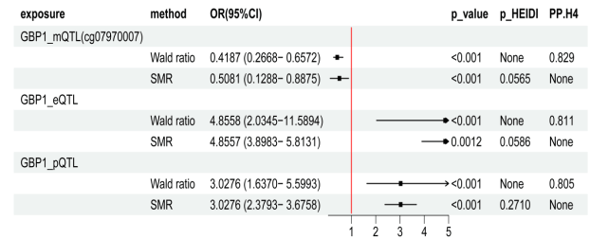 图4.ROC曲线+SHAP值排序+多组学数据MR验证编辑
图4.ROC曲线+SHAP值排序+多组学数据MR验证编辑
核心逻辑
通过综合机器学习算法:随机森林(RF)、岭回归(Ridge)等,并利用SHAP值来解释模型的决策过程,再结合多组学数据综合判断验证。挖掘并确定GBP1是EBV驱动ccRCC的核心生物标志物,且驱动作用是稳定可靠的。
5、转化价值落地:药物预测+分子对接
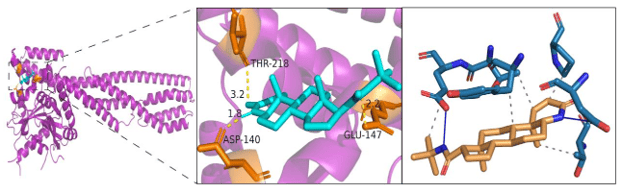 图5.分子对接模型编辑
图5.分子对接模型编辑
核心逻辑
基于核心靶点筛选临床可用药物,通过分子对接验证结合亲和力,为后续实验提供明确方向。
整合分析框架
为病毒致癌研究提供新范式
这项研究的核心价值,不仅在于揭示了EBV致ccRCC的具体机制,更在于构建了一套“从关联到靶点”的整合分析流程:
1、因果推断层
MR排除混杂,明确病毒与疾病的因果关系
2、细胞定位层
scRNA-seq+CellChat解析免疫细胞亚群及细胞间通讯,结合两步MR中介分析,明确免疫细胞的介导作用
3、基因筛选层
多算法机器学习+SHAP,实现核心基因精准定位
4、功能验证层
多组学交叉验证+分子对接,确保靶点可靠性与转化潜力
拜谱小结
从EBV暴露到ccRCC发生,其间隐藏着复杂的免疫与分子通路。本研究之所以能精准锁定核心靶点GBP1并发现老药新用的潜力,离不开多组学数据的深度整合与前沿生信方法的系统应用。
作为国内领先的多组学技术服务提供商,拜谱生物构建了“全流程闭环的多组学生信分析体系”,全面支撑从机制发现到靶点验证的科研全周期需求。无论是基于公共数据库的孟德尔随机化与中介分析,还是单细胞转录组深度解析、机器学习驱动的靶点筛选,贯穿“因果推断→靶点筛选→转化验证”,助力科研从数据走向机制、从机制迈向转化。
未来,拜谱生物将持续以高通量检测平台+智能化生信解决方案,助力科研工作者穿透数据迷雾,将每一个潜在的生物学信号转化为可解释、可验证、可转化的科学突破。让机制研究不止于发表,更走向临床价值的实现。
参考文献
Zhu G, Tan C, Li Y. GBP1 as a machine learning-prioritized biomarker and therapeutic target for epstein-barr virus-induced clear cell renal cell carcinoma: multi-omics causal validation. Int J Surg. 2025 Dec 10. doi: 10.1097/JS9.0000000000004393. Epub ahead of print. PMID: 41376480.