

心肌纤维化是众多心脏疾病不良预后的关键因素,目前缺乏直接针对成纤维细胞的特效治疗。
近日,南京医科大学季勇教授等人在Circulation发表题为“S-Nitrosylation of Pyruvate Kinase Isoform 2 Drives Cardiac Fibrosis by Promoting Mitochondrial Fission”的研究文章,不仅揭示了心肌纤维化的全新发病机制,还发现了一款已获批药物的新用途,为这一难题带来了突破性解决方案。

研究结果
01、核心靶点
SNO-PKM2在心肌纤维化中特异性升高
研究通过S-亚硝基化修饰蛋白质组学分析,从横向主动脉缩窄(TAC)小鼠、自发性高血压大鼠心脏组织中,鉴定出54个共同S-亚硝基化蛋白,其中PKM2因仅高表达于CFs、心肌细胞中未检测到,成为核心研究对象。验证显示,心衰患者心肌组织中SNO-PKM2水平显著高于非心衰供体;TAC小鼠、血管紧张素II(Ang II)刺激的CFs中,SNO-PKM2均明显升高,NO供体可直接诱导其升高,抗坏血酸能逆转该效应,证实NO是修饰来源。这一发现首次明确SNO-PKM2是心肌纤维化的特异性修饰蛋白,为机制研究锁定核心靶点。
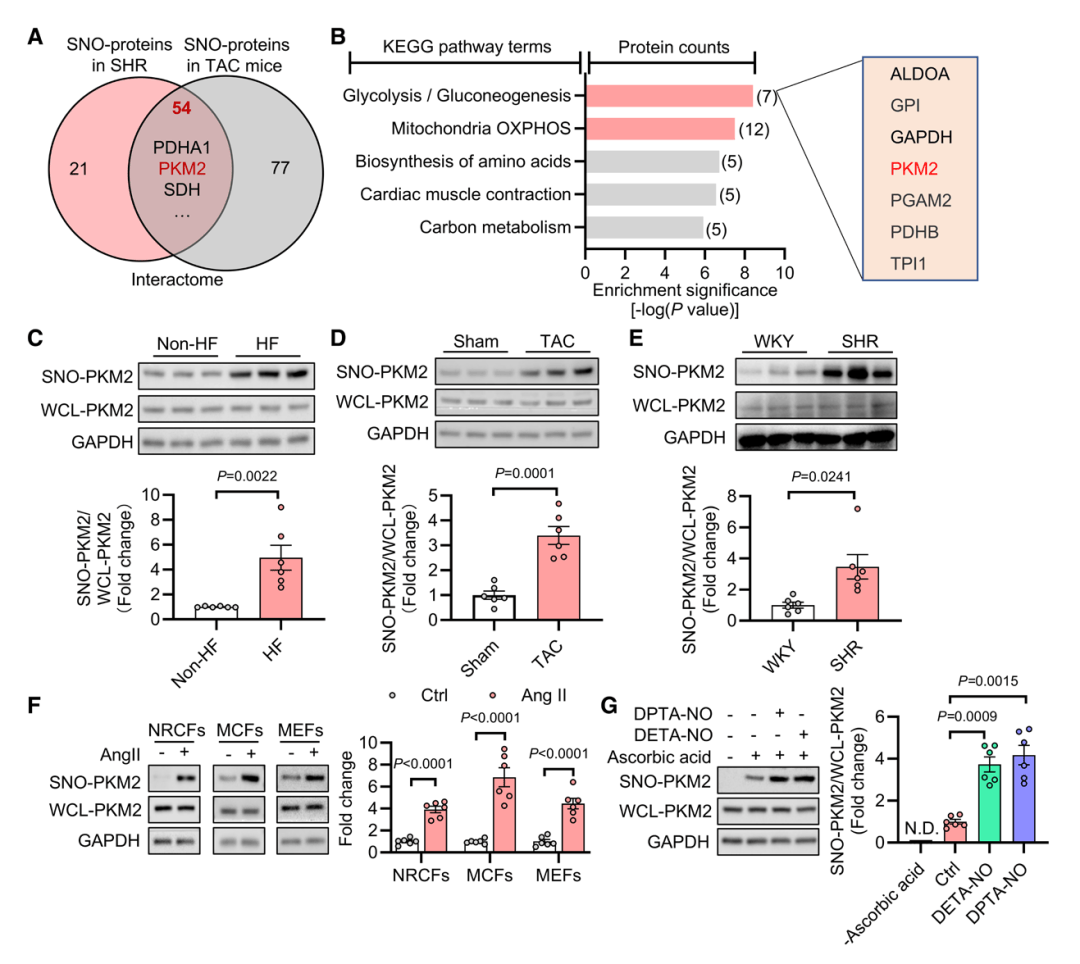 图1 SNO-PKM2在心脏纤维化过程中升高
图1 SNO-PKM2在心脏纤维化过程中升高
02、修饰位点
Cys49和Cys326是关键功能位点
通过液相色谱-串联质谱分析,精准鉴定PKM2的半胱氨酸49(Cys49)和326(Cys326)为SNO修饰关键位点。功能验证显示,沉默内源性PKM2后,通过表达Cys49/326S双突变体(MUT)可完全阻断AngII诱导的SNO-PKM2升高,并抑制CFs激活标志物α-SMA表达,且不影响基线状态下PKM2的四聚化和酶活性。
 图2 PKM2的S-亚硝基化发生在Cys49/326位点
图2 PKM2的S-亚硝基化发生在Cys49/326位点
03功能效应
SNO-PKM2抑制PKM2活性驱动CFs激活
结构分析显示Cys49和Cys326位于PKM2催化结构域,修饰后直接降低PKM2酶活性,破坏其高活性四聚体结构(双突变体可恢复)。功能上,SNO-PKM2通过抑制PKM2,引发糖酵解受阻、磷酸戊糖途径激活的代谢重编程,同时导致线粒体耗氧率降低、ROS升高、膜电位丢失,最终推动CFs增殖及向肌成纤维细胞分化。心衰患者心肌组织中PK酶活性显著低于供体,验证了这一功能改变。
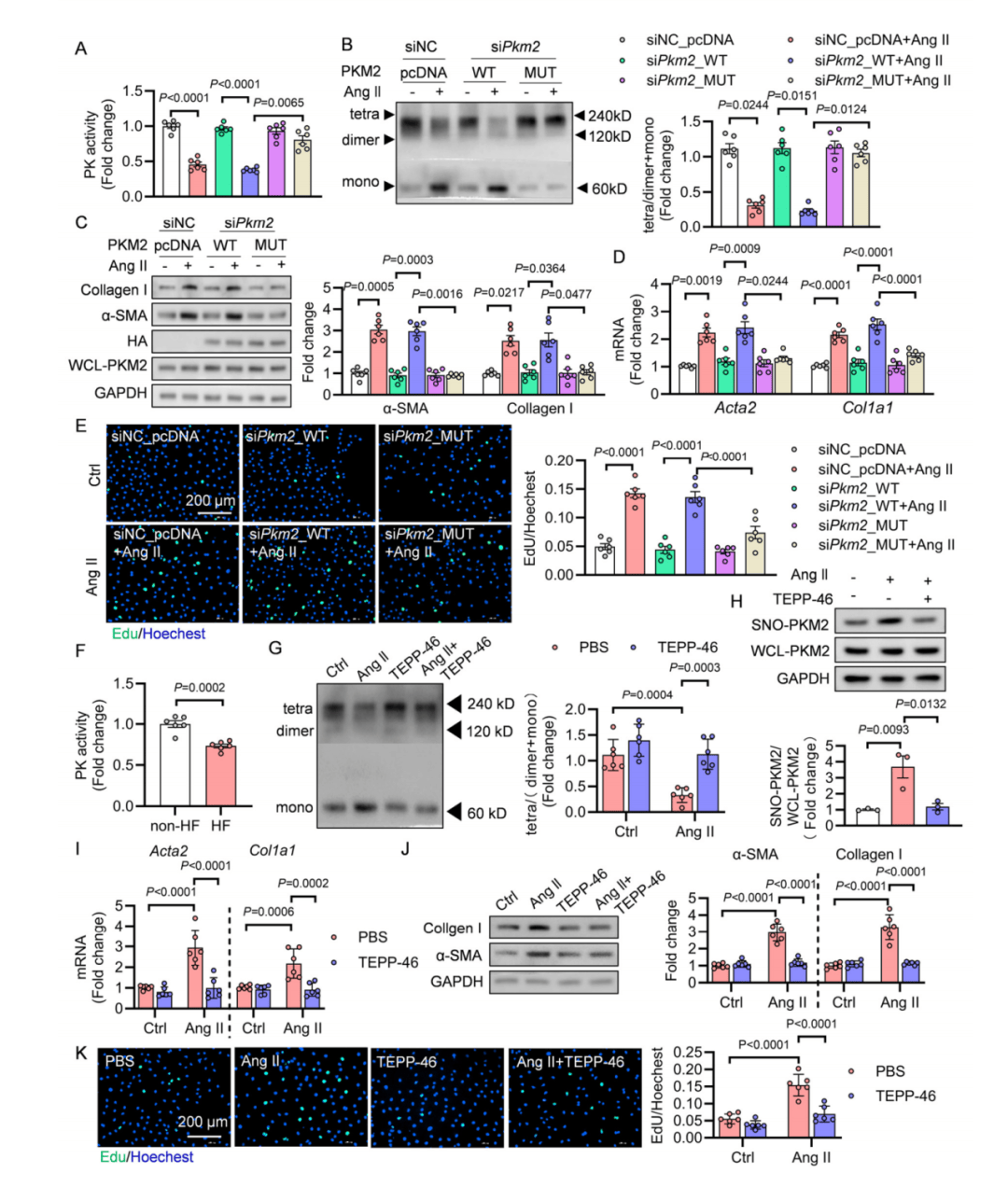 图3 SNO-PKM2促进心脏成纤维细胞向肌成纤维细胞分化
图3 SNO-PKM2促进心脏成纤维细胞向肌成纤维细胞分化
04、分子机制
GSN依赖途径驱动线粒体过度分裂
通过免疫共沉淀结合质谱分析,筛选出与PKM2相互作用的凝溶胶蛋白(GSN)为核心下游分子。实验证实,AngII刺激后,PKM2与GSN结合减弱,GSN与动力相关蛋白1(DRP1)结合增强。机制上,SNO-PKM2通过降低PKM2四聚化,释放GSN,促进DRP1-S616位点磷酸化及线粒体转运,引发线粒体过度分裂,最终激活CFs。敲低GSN或抑制CaMKII可阻断该过程,逆转纤维化表型。
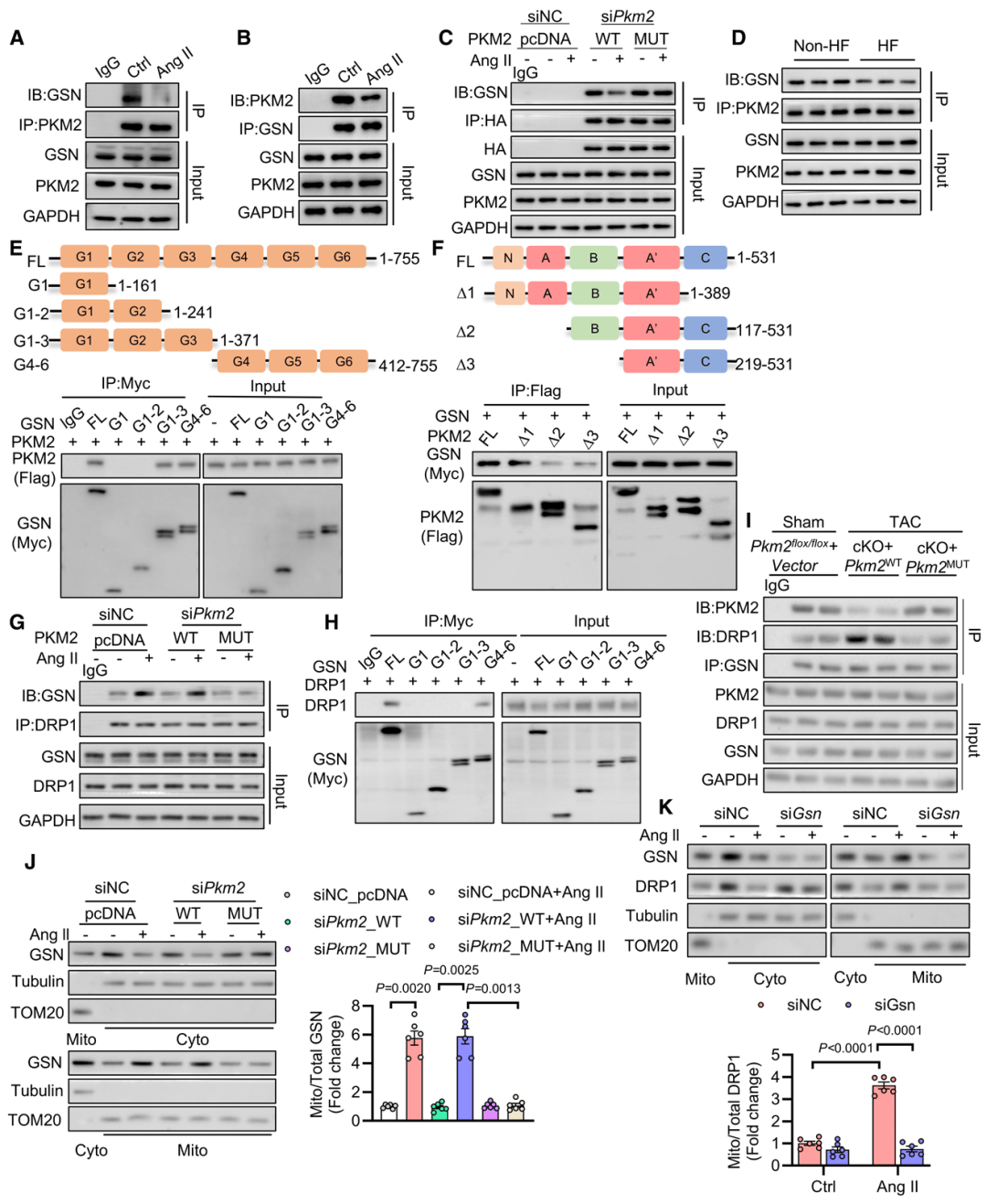 图4 SNO-PKM2以凝溶胶蛋白依赖性方式介导DRP1的线粒体转位
图4 SNO-PKM2以凝溶胶蛋白依赖性方式介导DRP1的线粒体转位
5、体内验证
PKM2敲除加重纤维化,突变体可拯救
构建CFs特异性PKM2条件性敲除(cKO)小鼠,TAC手术后发现:cKO小鼠心脏收缩/舒张功能恶化(EF、FS降低,E/E’升高),心肌肥大、胶原沉积显著增加,证实CFs中PKM2缺失加重纤维化。向cKO小鼠转染SNO抵抗型PKM2双突变体后,上述病理表型均显著逆转,而转染野生型PKM2无此效果,同时心肌组织中SNO-PKM2水平、线粒体分裂程度恢复正常。
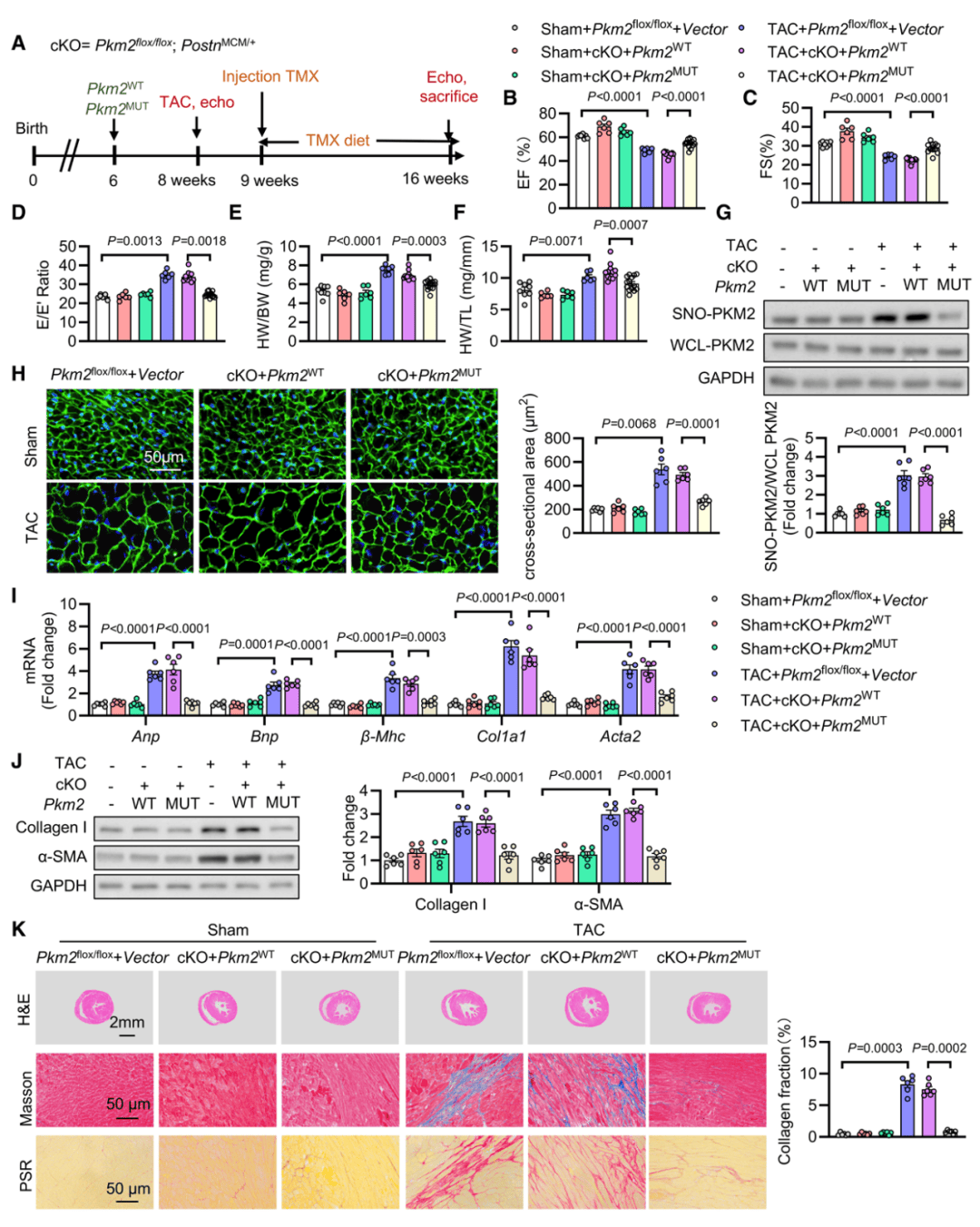 图5 SNO-PKM2可诱导TAC小鼠发生心脏肥大和心脏纤维化
图5 SNO-PKM2可诱导TAC小鼠发生心脏肥大和心脏纤维化
06、治疗潜力
mitapivat剂量依赖性缓解纤维化
体外实验显示,mitapivat剂量依赖性升高PKM2活性,降低纤维化标志物表达;体内实验中,TAC小鼠给予mitapivat(10/50mg/kg,每日两次)后,心脏功能、心肌肥大及纤维化均显著改善(P<0.0001),高剂量可使EF、FS接近正常水平。此外,mitapivat兼具预防(TAC后立即给药)和治疗(TAC后2周给药)作用,且无明显肝肺肾副作用。
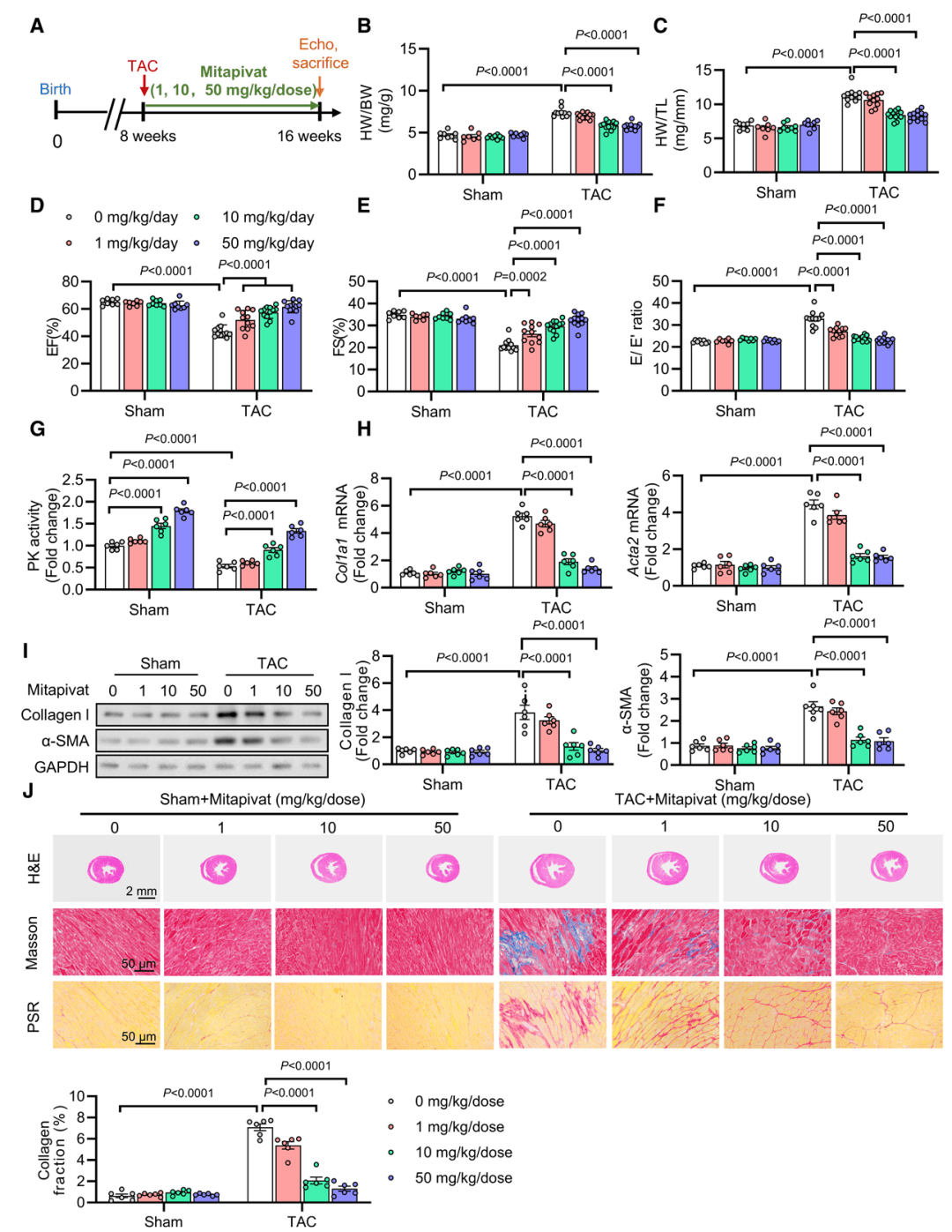 图6 mitapivat预处理减轻了TAC诱导的心肌纤维化和心力衰竭
图6 mitapivat预处理减轻了TAC诱导的心肌纤维化和心力衰竭
文章小结
本研究首次揭示“NO-iNOS-SNO-PKM2(Cys49/326)-GSN-DRP1-线粒体分裂-心肌纤维化”的完整机制:PKM2的Cys49和Cys326位点亚硝化修饰,通过抑制其活性与四聚化、干扰GSN相互作用,驱动DRP1介导的线粒体过度分裂,最终激活CFs。PKM2激活剂(尤其是mitapivat)可阻断该病理通路,有效缓解纤维化。mitapivat已获批临床应用,安全性明确,有望快速推进至心肌纤维化临床研究,为这一缺乏靶向治疗的疾病提供新策略。
拜谱小结
该研究首次揭示SNO-PKM2(Cys49/326位点)通过GSN-DRP1通路驱动线粒体过度分裂,最终激活心肌成纤维细胞引发心肌纤维化;FDA获批药物mitapivat可通过激活PKM2阻断该通路,为心肌纤维化提供新治疗策略。
拜谱生物可提供完善成熟的蛋白质组学、修饰组学、代谢组学、转录组学等多组学产品技术服务体系,整合多组学数据进行深入挖掘分析,全面解析机制机理;拜谱生物基于最新款Orbitrap™ Astral™ Zoom质谱仪打造高灵敏检测平台以及Cell顶刊背书的Cys-Tag技术,所需样品量降低至常规方法的10%,且修饰位点检测数量提升20%,可提供涵盖棕榈酰化、亚硝基化、谷胱甘肽化、硫巯基化、次磺酸化、氧化还原、游离巯基等全谱半胱氨酸修饰分析服务,积累了丰富的项目经验,助力高分文章发表,欢迎咨询!
参考文献
Luo S, Ye D, Zhang Y, et al. S-Nitrosylation of Pyruvate Kinase Isoform 2 Drives Cardiac Fibrosis by Promoting Mitochondrial Fission. Circulation. 2025.