

恶性黑色素瘤(MM)是一种以快速进展和转移潜能为特征的癌症,对全球健康构成重大威胁,导致全球近80%的皮肤癌死亡病例。
近日,川北医学院附属医院李玲团队在Chem. Eng. J.上发表题为“Nature-Inspired cell membrane-coated artificial biocatalysts with Os-single-atom sites and multienzyme-Mimetic activities for targeted tumor therapy”的论文。明确锇(Os)单原子与氧空位(Ov)的协同作用,以及“ROS爆发→线粒体损伤→凋亡通路激活”的治疗路径,为开发肿瘤治疗及其他ROS相关疾病领域的高性能活性氧催化材料提供了新思路。拜谱生物为该研究提供了转录组学检测服务。

英文标题:Nature-Inspired cell membrane-coated artificial biocatalysts with Os-single-atom sites and multienzyme-Mimetic activities for targeted tumor therapy(Chemical Engineering Journal IF:13.2)
中文标题:受自然启发的细胞膜包覆人工生物催化剂(具有锇单原子位点及多酶模拟活性)用于靶向肿瘤治疗
客户单位:川北医学院附属医院
研究材料:小鼠肿瘤组织
拜谱提供技术:转录组学
技术路线:

一、研究结果
01.人工生物催化剂的合成与表征
作者设计了一种新型高效人工生物催化剂。扫描电子显微镜(SEM)和高分辨透射电镜(HR-TEM)显示,该催化剂呈现球形结构且具有超小纳米尺度。动态光散射(DLS)技术证实了CCM在OsCu-Ov上的成功包覆,能量色散光谱(EDS)图谱显示单原子位点的形成(图1 a-f),X射线光电子能谱(XPS)和X射线吸收谱(XAS)技术表征结果证明人工生物催化剂的成功制备(图2 a-g)。
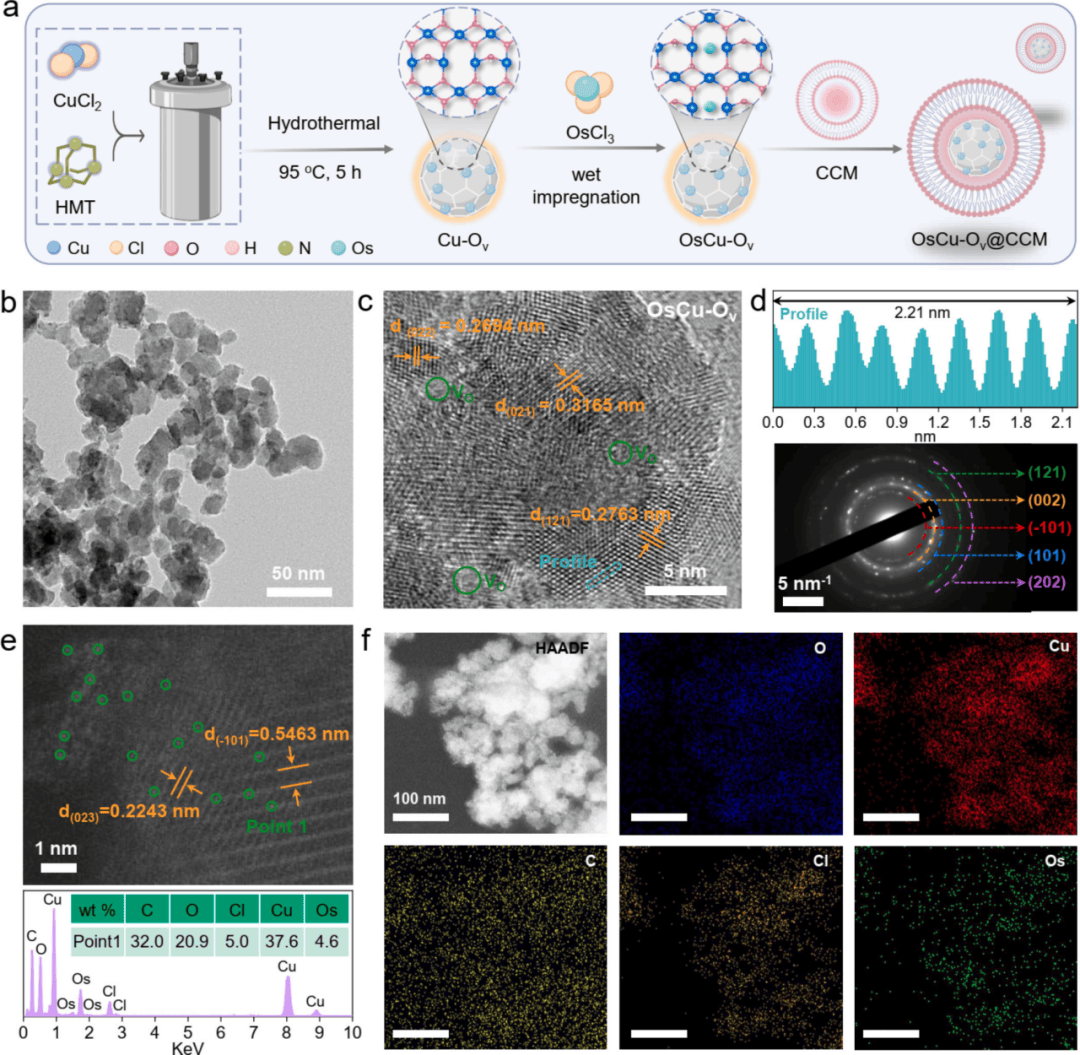 图1 OsCu-Ov人工生物催化剂的设计和结构表征
图1 OsCu-Ov人工生物催化剂的设计和结构表征
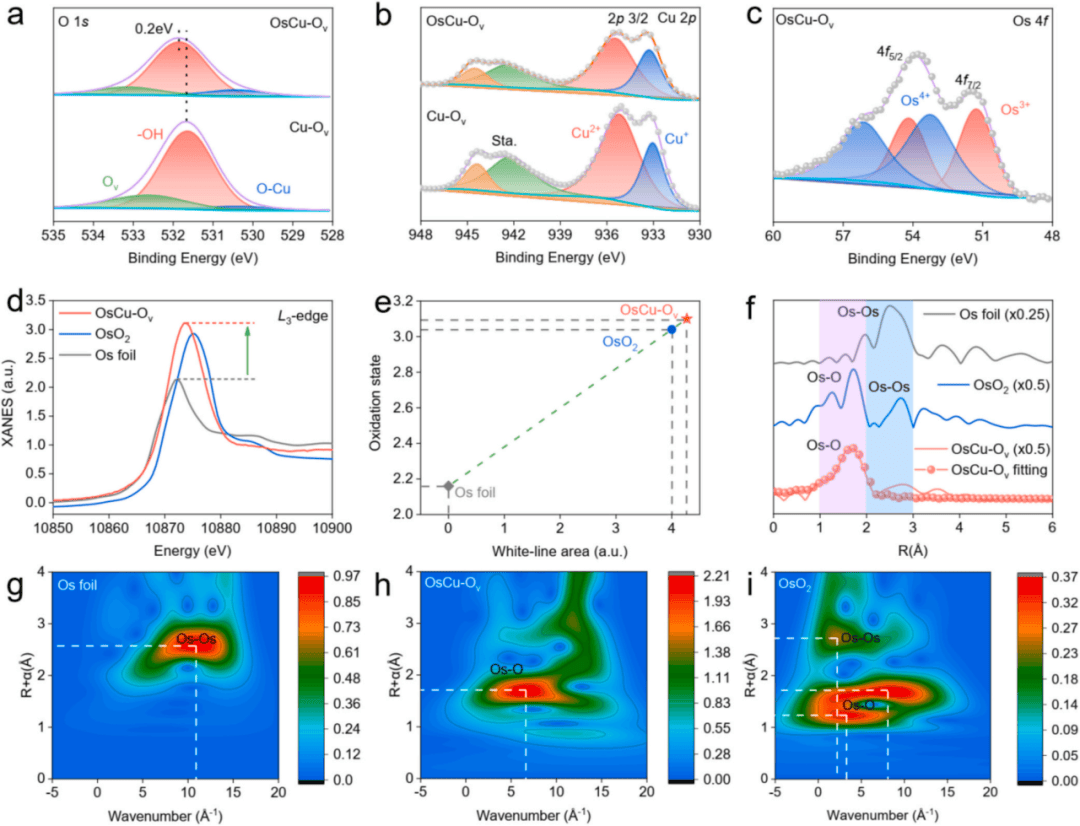 图2 利用XPS和XAS对生物催化剂进行电子结构分析
图2 利用XPS和XAS对生物催化剂进行电子结构分析
02.人工生物催化剂的酶模拟活性
在当前纳米材料中,OsCu-Ov生物催化剂展现出优异的活性氧催化活性,不同反应条件下均保持高效产氧能力(图3 a-h)。
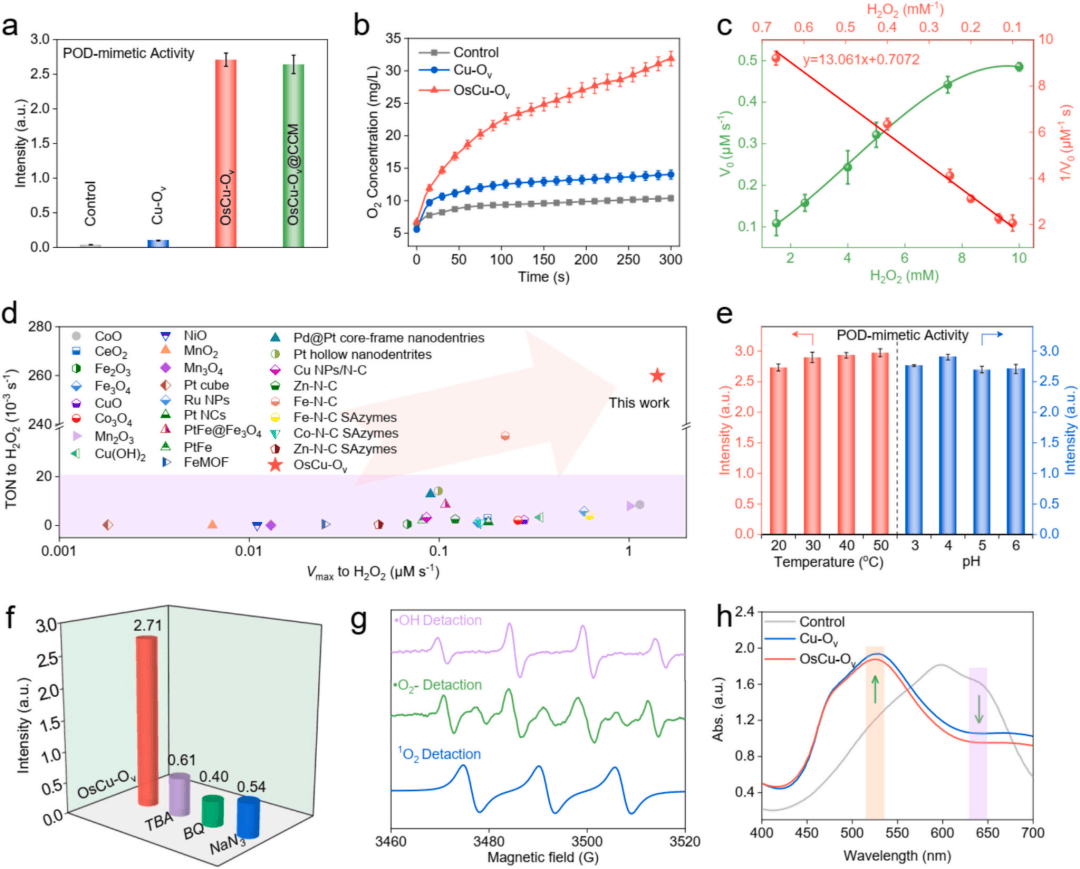 图3 OsCu-Ov人工生物催化剂的酶模拟活性物质ROS生成活性
图3 OsCu-Ov人工生物催化剂的酶模拟活性物质ROS生成活性
03.体外抗肿瘤能力验证
共聚焦激光扫描显微镜,流式细胞术,蛋白质印迹结果表明OsCu-OV@CCM可能通过E-cadherin介导的途径更有效地靶向和进入肿瘤细胞(图4 a-c)。CCK-8检测结果显示轻微毒性作用,40μg mL−1浓度效果最佳。共染色实验结果显示OsCu-Ov@CCM组的死细胞比例高于OsCuOv治疗组,ROS升高,细胞凋亡率升高(图4 d-h)。
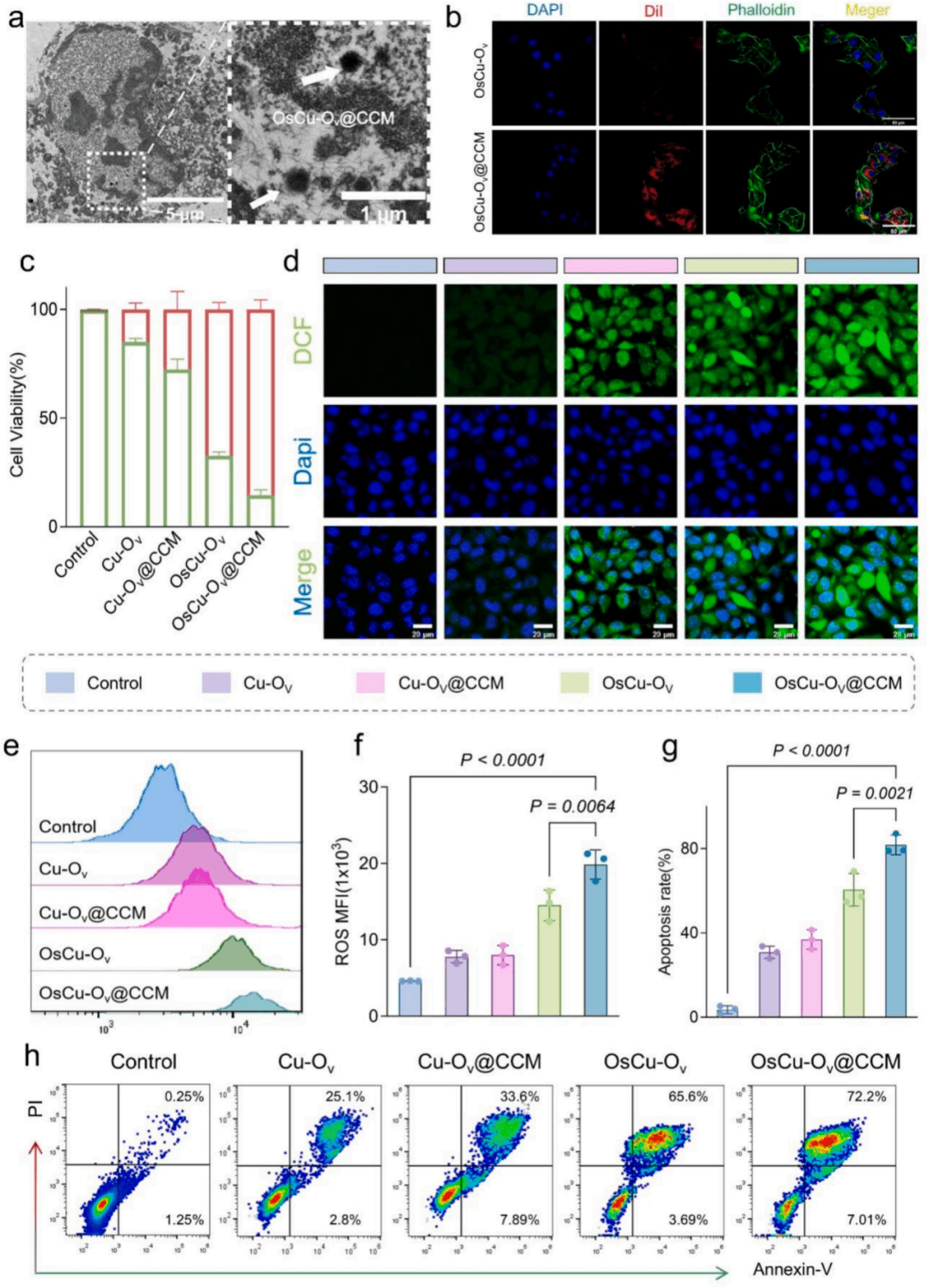 图4 体外细胞试验验证OsCu-Ov@CCM的抗肿瘤能力
图4 体外细胞试验验证OsCu-Ov@CCM的抗肿瘤能力
OsCu-Ov@CCM组线粒体Calcein-AM荧光被CoCl₂显著淬灭,证明mPTP开放,JC-1染色显示,OsCu-Ov@CCM 组红色聚集体转为绿色单体,ΔΨm崩溃(图5 a-d)。蛋白质印迹分析裂解型半胱天冬酶-3和Bax水平显著升高(图5 g-j)。
 图5 线粒体损伤检测
图5 线粒体损伤检测
04.体内抗肿瘤疗效实验
OsCu-Ov@CCM组肿瘤重量、体积热图显示全程无明显增长,H&E染色显示出最高比例的凋亡细胞。活体成像系统显示瘤内给药后该材料在肿瘤内维持高浓度达24小时,随后主要通过肾脏和肝脏途径被清除(图6b-g)。
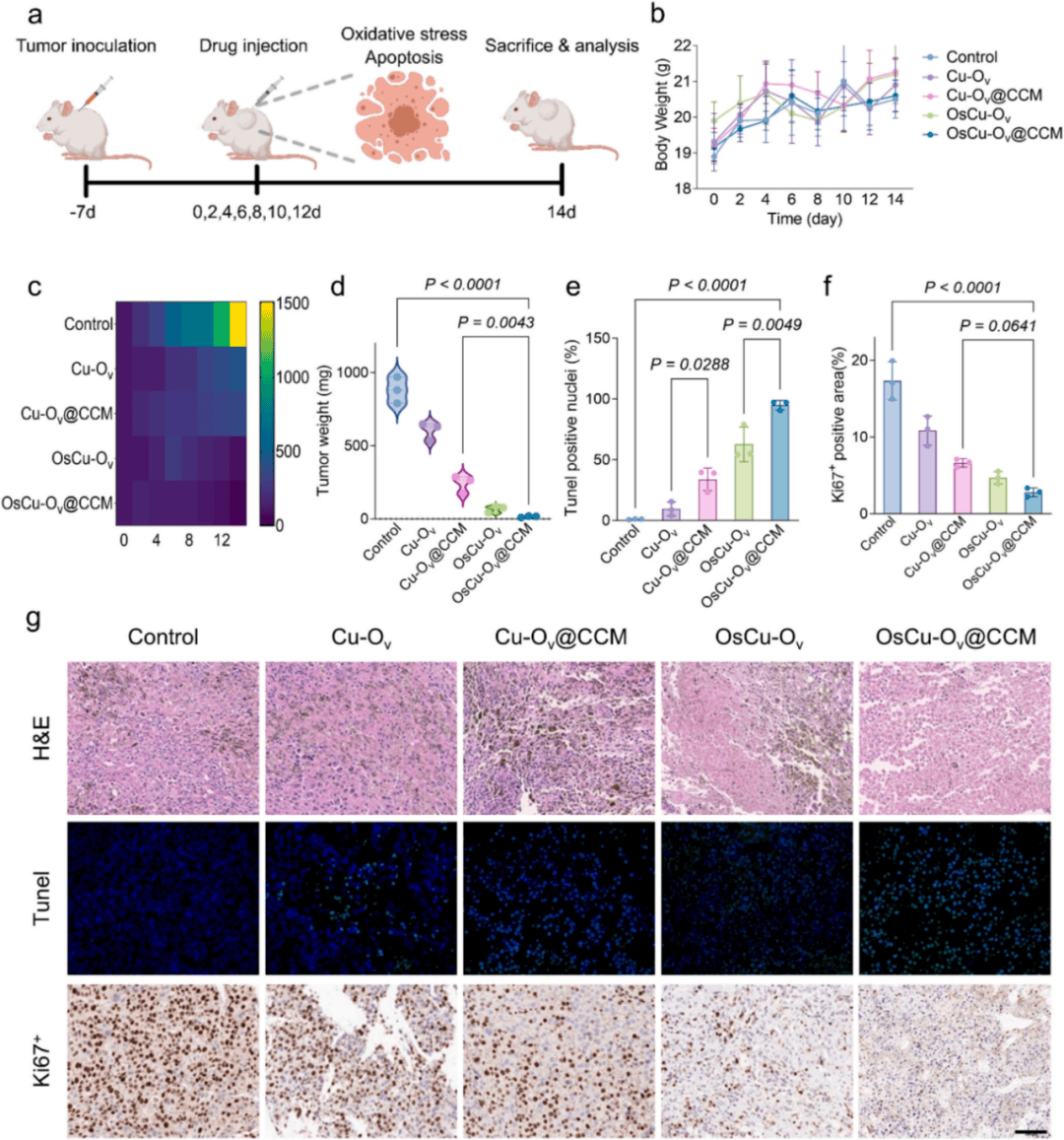 图6 体内抗肿瘤治疗
图6 体内抗肿瘤治疗
05.肿瘤杀伤机制探索
对照组、CuOv@CCM组和OsCu-Ov@CCM组小鼠肿瘤组织进行转录组学测序,OsCu-Ov@CCM上调的基因主要集中在与细胞凋亡相关的多个信号通路中,呈现下调趋势(图7 a-e)。基因集富集分析(GSEA)提示OsCu-Ov@CCM可能破坏线粒体内膜蛋白复合体及线粒体蛋白复合物,与多个调控细胞凋亡的信号通路活性增强相关,包括PI3K-Akt信号通路、钙信号通路和TGF-β信号通路(图7 f-h)。这些发现表明OsCu-Ov@CCM能够调控关键的细胞通路,有望改善多发性骨髓瘤的治疗效果。
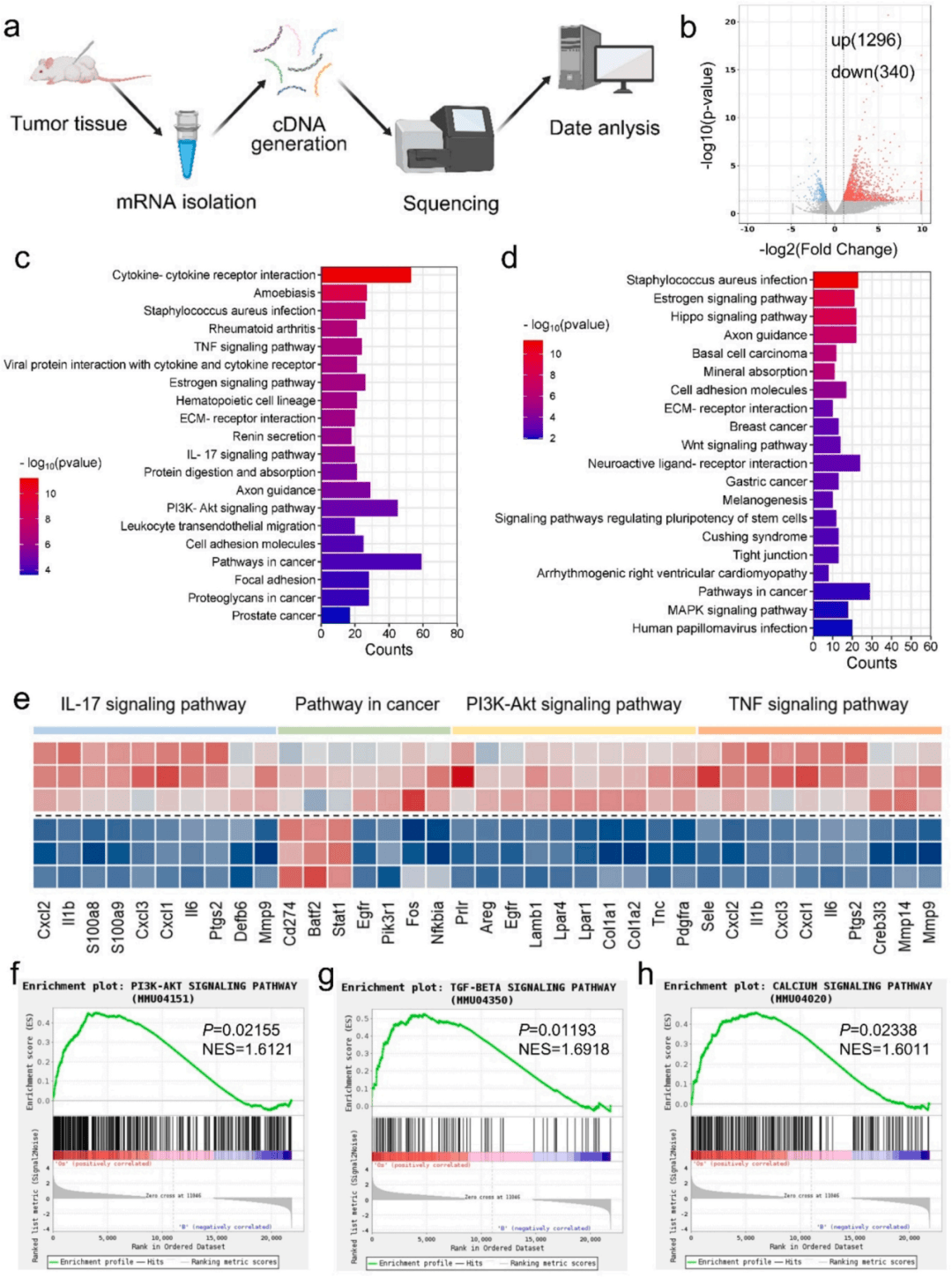 图7 OsCu-Ov@CCM杀瘤作用的机理研究
图7 OsCu-Ov@CCM杀瘤作用的机理研究
二、文章小结
本研究证实,开发的新型细胞膜包覆酶模拟物OsCu-Ov@CCM(含单原子锇活性中心与Ov结构)是理想的纳米平台,能精准模拟产生活性氧的酶功能,为肿瘤微环境中的恶性黑色素瘤治疗提供高效靶向方案(图 8)。
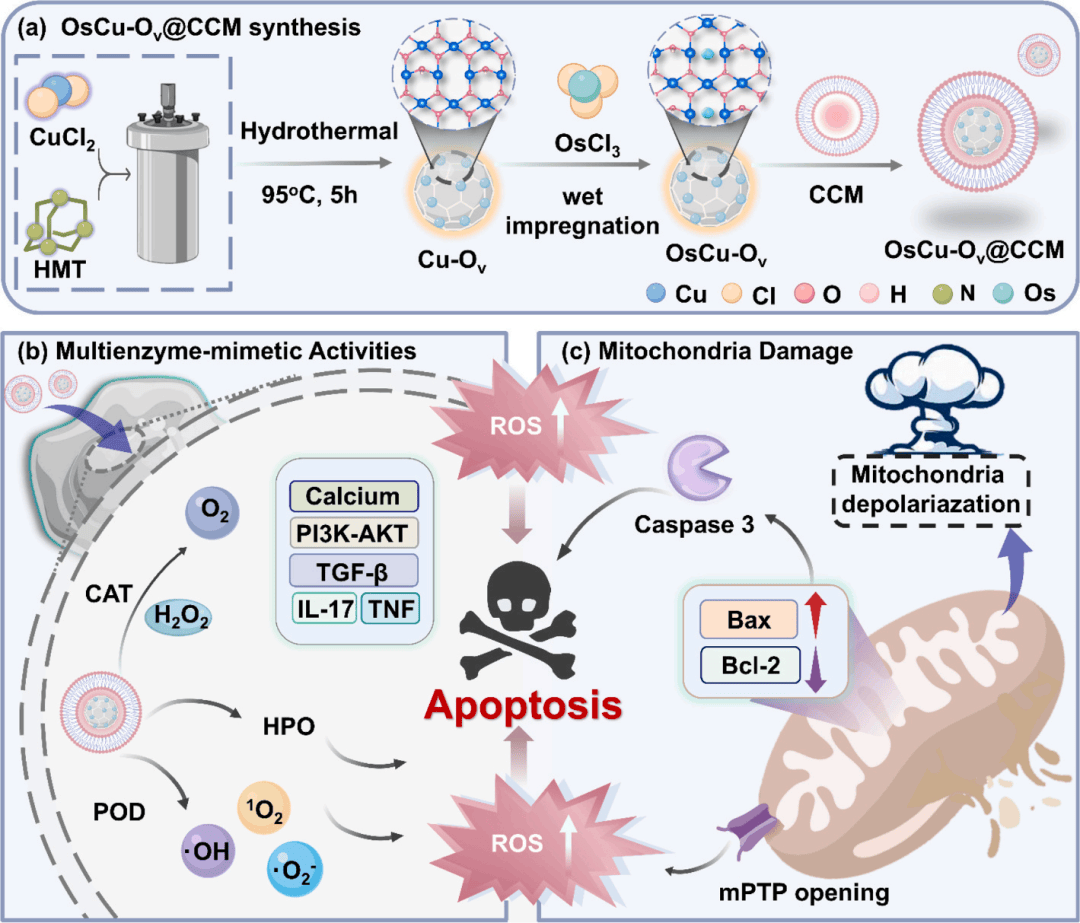 图8 OsCu-Ov@CCM治疗恶性黑色素瘤的机制示意图
图8 OsCu-Ov@CCM治疗恶性黑色素瘤的机制示意图
三、拜谱小结
本研究明确了Os单原子与Ov的协同作用,以及“ROS爆发→线粒体损伤→凋亡通路激活”的治疗路径,为开发肿瘤治疗及其他ROS相关疾病领域的高性能活性氧催化材料提供了新思路。拜谱生物为其提供了转录组学检测分析。拜谱生物已研发完成并建立了完善成熟的转录组学、蛋白组学、翻译后修饰组、代谢组学以及多组学联合产品技术服务体系,助力发表高分文献,欢迎致电咨询!
参考文献:Jiawei W, Jing W, Zijun M, et,al. Nature-Inspired cell membrane-coated artificial biocatalysts with Os-single-atom sites and multienzyme-Mimetic activities for targeted tumor therapy. Chemical Engineering Journal.doi.org/10.1016/j.cej.2025.166190.