

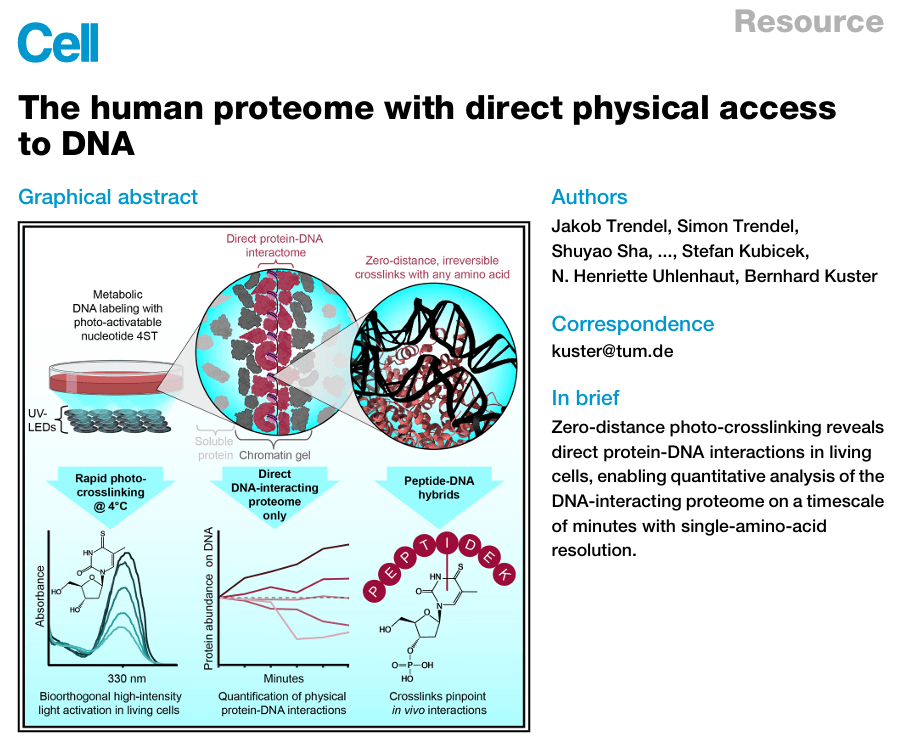
在人类细胞中,DNA充满了组蛋白、RNA和染色质相关蛋白,形成粘性凝胶。在任何给定时刻,只有蛋白质组的一个子集可以结合DNA并组织其结构、转录、复制、修复和其他基本分子功能。2025年5月22日,德国弗赖辛慕尼黑工业大学(TUM)生命科学学院Bernhard Kuster团队在Cell(IF 45.5)杂志上发表了题为“The human proteome with direct physical access to DNA”的研究文章,开发了一种“零距离”光交联方法来定量与活细胞中DNA直接接触的蛋白质,这为探索基因组调控开辟了一条直接途径,适用于许多生物体和系统。
研究结果
1、从光敏培养细胞中提取DNA交联蛋白质
为了分离光交联蛋白质-DNA复合物用于LC-MS分析,作者开发了一种变性纯化方案,可从DNA中去除非交联蛋白质,仅在照射时通过直接基因组接触富集DNA交联蛋白质。用TRIZOL提取染色质并去除被捕获的非交联蛋白,然后将其重新溶解以进行RNase消化。通过超声剪切所得蛋白质交联DNA的提取物,在硫氰酸胍中煮沸变性,并在二氧化硅离心柱上剧烈洗涤以去除非交联蛋白质直至完成。通过核酸酶处理从DNA中释放光交联蛋白,并进行胰蛋白酶消化用于LC-MS分析。该方法命名为蛋白质交联DNA提取或XDNAX。
 图1.蛋白质交联DNA提取或XDNAX流程图(图源:Trendel, et al., Cell 2025)
图1.蛋白质交联DNA提取或XDNAX流程图(图源:Trendel, et al., Cell 2025)
2、可直接接触DNA的蛋白质图谱
将光交联方法应用于MCF7细胞,发现了1,805种候选蛋白,其中1,191种存在于3个或更多次重复中。60%的DNA相互作用组带有核酸结合的GO注释,在缺乏核酸结合注释的蛋白质中,最大的贡献来自核纤层蛋白,其次是参与染色质组织和细胞分裂的蛋白质(图2)。
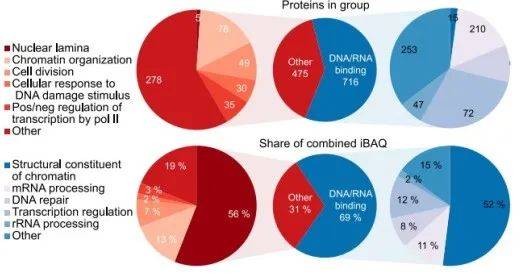 图2 . 可直接接触 DNA 的蛋白质(改自:Trendel, et al., Cell 2025)
图2 . 可直接接触 DNA 的蛋白质(改自:Trendel, et al., Cell 2025)
图3总结了DNA相互作用组所隐含的蛋白质-DNA界面及其包含的核苷酸交联肽。这包括由于(1)球状DNA结合结构域、(2)DNA 结合无序区(IDR)和(3)由于与其他蛋白质(例如组蛋白结合蛋白)、RNA(例如剪接因子)或相分离区室(例如核仁蛋白)相互作用而导致的环境接近。
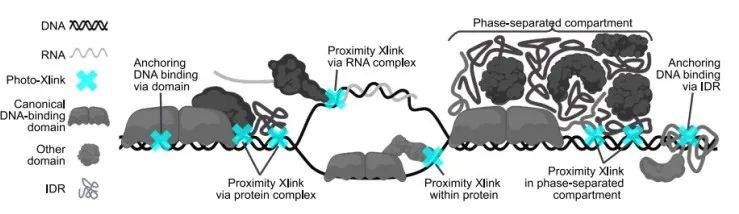 图3 . 可直接接触 DNA的结构域(改自:Trendel, et al., Cell 2025)
图3 . 可直接接触 DNA的结构域(改自:Trendel, et al., Cell 2025)
3、定量细胞扰动期间与DNA结合的转录因子
雌激素受体α(ESR1)驻留在胞质溶胶中,直到遇到其配体,触发易位到细胞核,在那里它与基因组中的特定区域结合以激活特定的转录程序。将血清饥饿的MCF7细胞暴露于高剂量雌激素(10 nM 17β-雌二醇)45分钟,与模拟处理的对照细胞比较它们的DNA相互作用组(图4A)。其中,雌激素刺激后DNA相互作用组中的ESR1增加了30倍(图4B)。总的来说,在1,814个定量的蛋白质-DNA相互作用中,约有9%显示出超过2倍的显著变化,并观察到与ESR1具有相互作用的蛋白如POLR2A和SMARCA4等(图4B-C)。
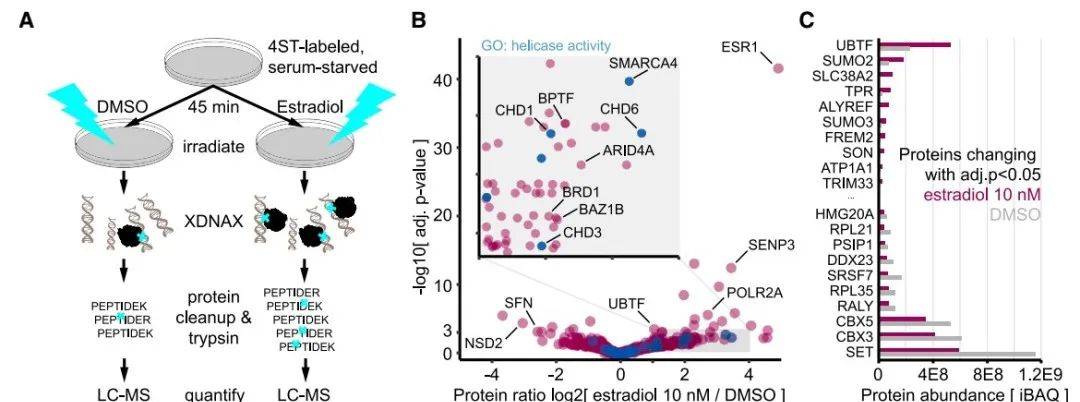 图4 雌激素处理乳腺癌细胞 DNA 相互作用组的定量比较(图源:Trendel, et al., Cell 2025)
图4 雌激素处理乳腺癌细胞 DNA 相互作用组的定量比较(图源:Trendel, et al., Cell 2025)
小结
研究进入基因组的蛋白质以了解它是如何被读取并付诸实践的,一直是科研人员一个长期的追求。基因组可及性主要以DNA为中心的角度进行研究,然而,到目前为止,染色质凝胶中的哪些蛋白质与DNA 发生物理相互作用尚不清楚。使用零距离光交联,可发现DNA相互作用组中的大多数蛋白质,XDNAX技术将作为蛋白质-DNA相互作用研究的强大工具。
拜谱小结
该研究基于LC-MS/MS蛋白质谱开发的XDNAX技术,实现了活细胞内蛋白质与DNA直接相互作用的精准捕获与定量分析,绘制了高分辨率的人类DNA互作蛋白图谱,为解析基因组调控网络提供了全新工具。拜谱生物作为一家国内领先的多组学服务公司,可提供完善成熟的蛋白质组学、修饰组学、代谢组学、转录组学等多组学产品技术服务体系,整合多组学数据进行深入挖掘分析,全面解析机制机理等,助力高分文章发表。欢迎咨询!
参考文献:
Trendel J, Trendel S, Sha S, Greulich F, Goll S, Wudy SI, Kleigrewe K, Kubicek S, Uhlenhaut NH, Kuster B. The human proteome with direct physical access to DNA. Cell. 2025 May 14:S0092-8674(25)00507-0. doi: 10.1016/j.cell.2025.04.037.