“战疫”新发现——蛋白质组学助力新冠临床标志物鉴定及相关发病机理表征
Plasma Proteomics Identify Biomarkers and Pathogenesis of COVID-19
研究方法:蛋白质组学
期刊:Immunity
影响因子:22.553
新冠肺炎(COVID-19)的爆发流行对全世界而言无疑是一场最为巨大的挑战,无数的科研工作者在前线给我们带来了诸多新冠病毒相关的研究,为这场“战疫”的胜利提供了无限可能。2020年 10月 20日,Immunity(IF=22.553)在线发表了中国科学院武汉病毒研究所,武汉市金银潭医院张定宇等团队最新新冠研究,团队通过血浆蛋白质组学结合机器学习等分析方法揭示了可能存在的新冠临床标志物以及疾病发生发展可能的机制。

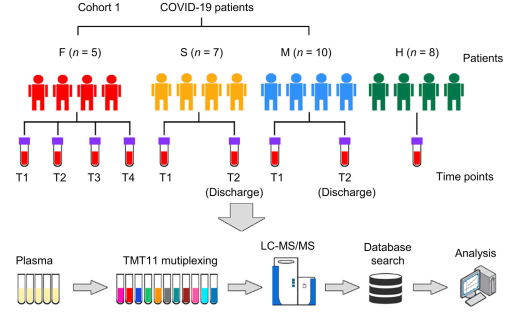
研究采集来自武汉金银潭医院的新冠患者的血液样本作为训练集,按疾病严重程度,分为四组。其中死亡病例组,按采样时间段分为 T1-T4四个时间段,每段5重复(F(n=5));重症病例组,分别采集T1,T2 两个时间段,每段7重复(S(n=7)),轻症病例组,分别采集T1,T2 两个时间段,每段 10 重复 (M(n=10))以及阴性对照组 8 重复(H(n=8))。血浆蛋白质组学采用 TMT 11-plex 蛋白质组标记技术,结合LC-MS/MS质谱分析手段,研究了不同疾病分型的差异蛋白表达谱。由于TMT 标记蛋白质组学受到标签通道的限制,本文实验样本个数多,需要平行标记多个试剂盒才能满足实验需求,为避免标记平行性可能引入的误差,研究者同时准备了所有样本的混样作为内标,标记于每个试剂盒,用于后期实验数据的质量评估及校正。同时,实验人员基于该蛋白质组学的结果构建了 SARS-CoV-2 相关的蛋白质组数据库用于后续疾病相关的组学研究。
训练集血浆蛋白质组学共鉴定到 8472 条肽段,其中6705 条肽段spectral counts ≥ 2,平均 spectral counts数为19.4。在蛋白水平上,共匹配到 860 个人源蛋白,472 个蛋白的匹配肽段数≥ 2,所有蛋白可平均匹配到 10 条肽段。该组学鉴定结果无论在蛋白水平或是肽段水平上,数据质量都是较高的。
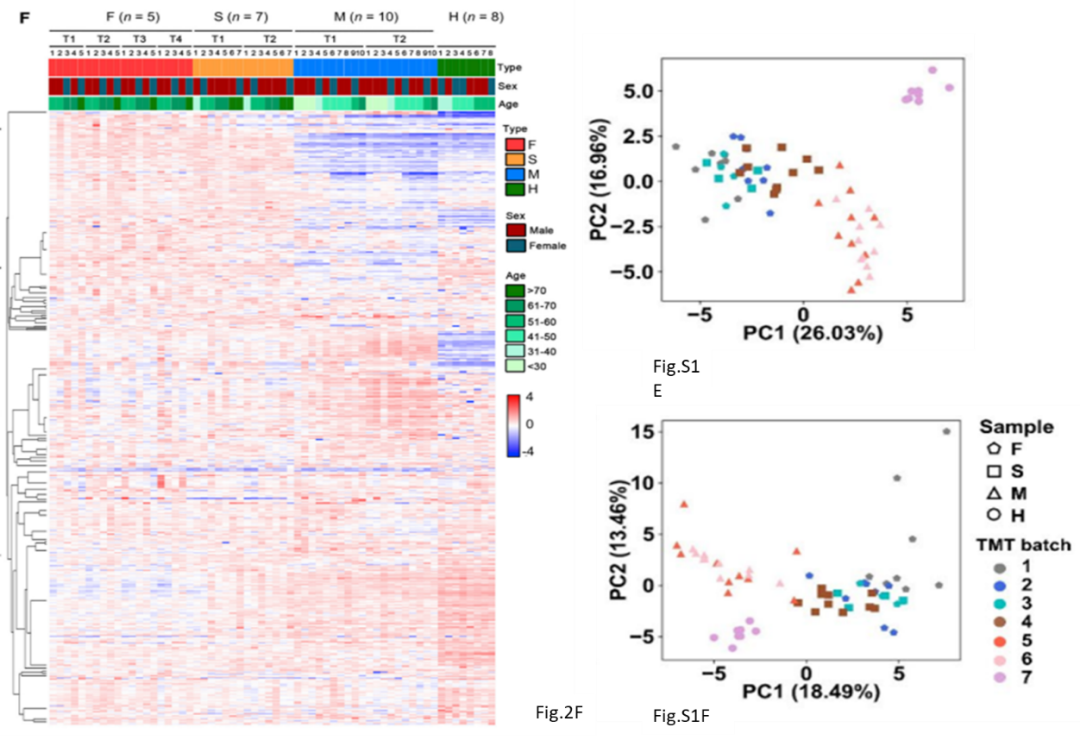
本文分别选用 530 个 > 70% 样本有定量值的蛋白(Fig.S1F)以及348 个所有样本均定量(Fig.SE)到的蛋白质的表达量进行 PCA (无监督聚类)分析,可以明显看出,H 以及 M组的表达趋势是不同于 S 以及 F组的。S 以及 F组差异蛋白表达成簇,不能有效区分,告诉了我们 COVID-19 病程从重症发展到致死过程中,蛋白组成是类似的,也同时提示我们通过该方法查找疾病预测标志物的可行性。基于 348 个全部定量蛋白表达量绘制的聚类热图(Fig.2F),更为直观的展示了疾病发展过程种蛋白表达的聚类情况,F 以及 S 组的蛋白表达谱与 M 以及 H 组相比是明显偏移的。
疾病相关组学大数据是为机制挖掘服务的,本文对 195 个差异表达蛋白进行 GO以及 KEGG 富集分析,COVID-19 相关差异蛋白相关的功能及机制主要富集在炎症反应,免疫细胞迁移,补体系统以及能量代谢等功能及机制通路上(Fig.3),为后续疾病深度机理机制研究提供了方向,其中血小板脱粒和补体凝血级联的富集程度最高。
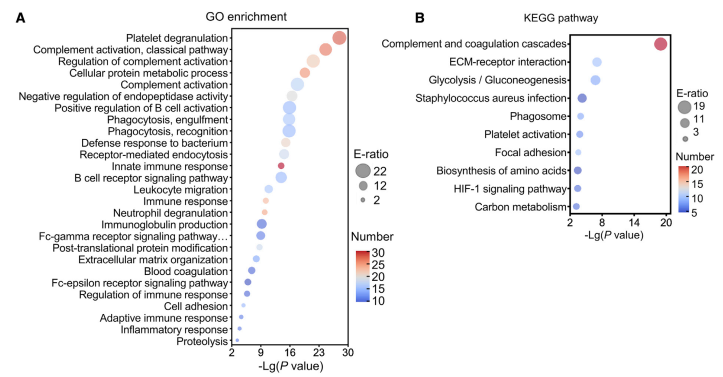
Fig.3
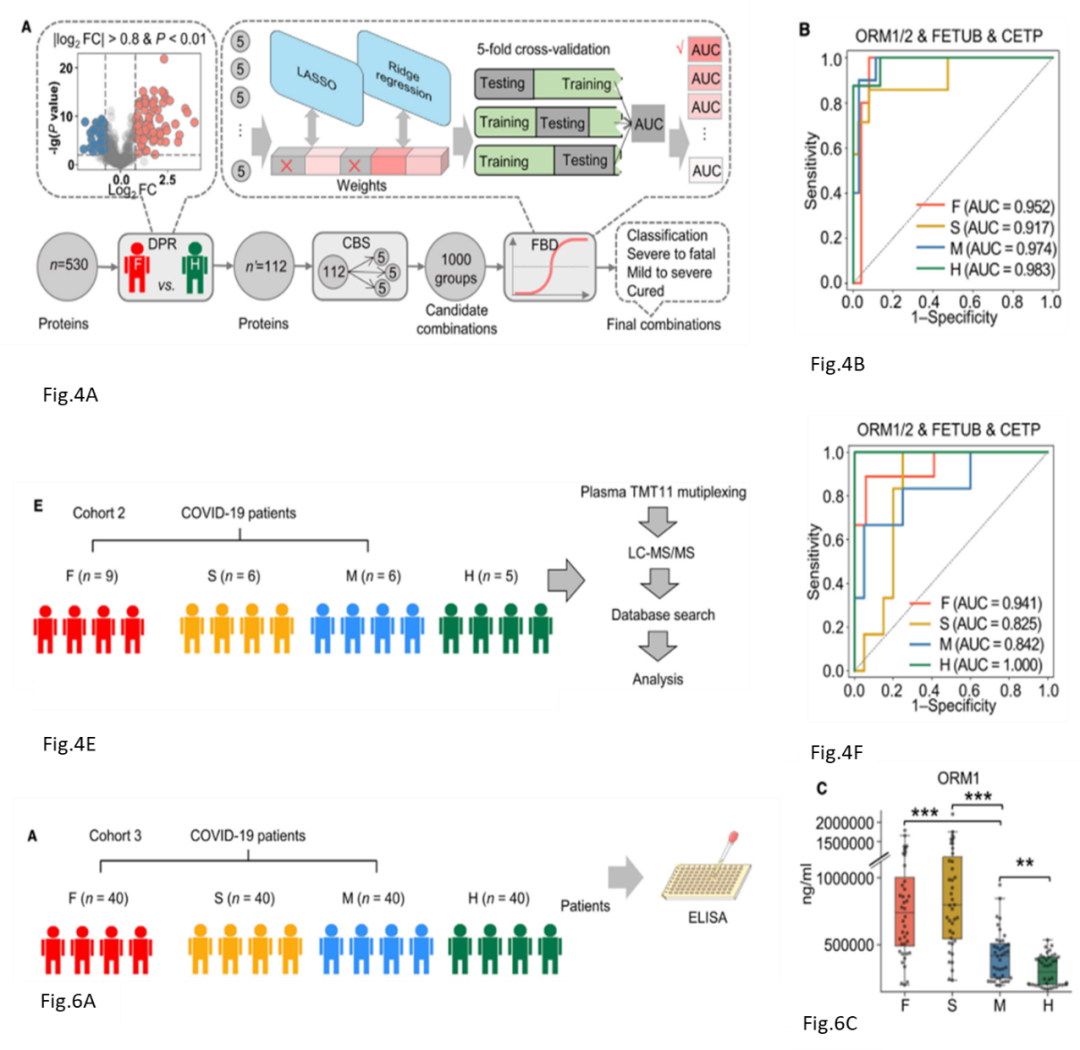
本文基于训练集数据开发了一套针对 COVID-19 优化的分子标志物算法(POC-19),组学数据在经历 1)差异蛋白筛选;2)候选标志物筛选;3)基于PLR(惩罚线性回归模型)算法确证候选生物标志物的三步数据处理后,可以高效找到 AUC 值最高的分子标志物(Fig.4A),本文队列1训练集数据通过该算法鉴定到ORM1/2,FETUB,CETP 四个预测标志物(Fig.4B)。研究人员为验证该算法可信度,重新设置了测试集队列进行 TMT 蛋白质组分析(9 例 F组样本, 6例 S 组样本,6 例 M 组样本以及 5 例 H 组样本),(Fig.4E)测试结果与实验结果一致(Fig.4F),上述候选的 4 个预测标志物在新队列中依旧表现良好,充分证明该模型用于 COVID-19 分子标志物筛选的可行性。
任何组学大数据均存在假阳性的结果,因此广谱的筛选均需靶向的手段辅以验证。本文重新设置验证集(分别每组收集 40 例 F, S, M以及 H 组样本),通过 Elisa 方法,对前文组学研究挖掘到的分子标志物进行靶向验证(Fig.6A)。结果发现ORM1, S100A8/S100A9, AZGP1, CFI以及 FETUB 表达趋势与组学结果一致(Fig.6C),该结果验证了组学结果的准确性,同时也为COVID-19 临床标志物的筛选提供了线索。
除文中所用 TMT 标记方法外,目前一类非数据依赖型的质谱检测手段- DIA (Data independent analysis)技术,对于临床血浆类存在明显高丰度蛋白样本的质谱检测提供了另一种可供选择的检测方法。
同时蛋白质靶向验证除了文中所采用经典的 Elisa 方法外,基于质谱的靶向 PRM 检测也是一种有效的靶向蛋白质验证方法。当实验过程中验证蛋白个数较多,或者无法得到靶标蛋白的特异性抗体,PRM 方法无疑是靶向蛋白验证的最优解。
SARS-CoV-2是一类全新的病毒,人类对它的认知是逐渐积累,逐步解析的,对于新冠的研究我们也会持续关注,跟进解读的,“战疫”的故事未完待续……
拜谱生物研发人员具备10年以上蛋白组学、修饰蛋白质组学、代谢组学、转录组学、基因组学等科研服务经验,提供各类样本分析方案与实验设计方案。已合作发表多篇高水平项目文章,欢迎来电咨询。
原文链接:
https://doi.org/10.1016/j.immuni.2020.10.008
拜谱生物团队解读
欢迎转发到朋友圈
如有转载、合作等需求,请联系拜谱生物公号客服